
شماره ۹۷۶
مارکرهای بیوشیمیایی استخوان
دکتر فریده رضی - آسیبشناس بالینی و تشریحی، عضو هیئت علمی پژوهشگاه علوم غدد و متابولیسم دانشگاه علوم پزشکی تهران
استخوان از نظر متابولیک یک بافت فعال است که بهطور مداوم تحتتأثیر دوجریان تشکیل استخوان جدید (bone formation) و بازجذب استــخوان قدیمی (bone resorption) قرار دارد.
این شرایط با توجه به فعالیت سلولهای استئوکلاست، استئوبلاست و استئوسیت که به ترتیب مسوول بازجذب، ساخت و نگهداری استخوان میباشند، تنظیم میشود. ضمن اینکه عوامل متعدد دیگری مانند میزان ویتامینPTH،D هورمونهای استروئیدی، میزان کلسیم و فسفر و همچنین عوامل موضعی مانند سیتوکینها و عوامل رشد نیز بر آن تاثیر میگذارند.
ارزیابی وضعیت استخوان از راههای مختلف مانند بررسی تراکم استخوان، تصاویر رادیولوژی و نیز مارکرهای بیوشیمیایی استخوان امکانپذیر است که مارکرهای بیوشیمیایی زودتر از سایر روشهای فوق، تغییرات را نشان داده و بیانگر وضعیت اسکلتی سیستمی میباشند. ارزشبالینی مارکرهای بیوشیمیایی استخوان عمدتاً درشناسایی افراد با turnover زیاد استخوان، بررسی احتمال شکستگی در زنان بعد از منوپوز و ارزیابی پاسخ به درمان در بیماران مبتلا به استئوپوروز، پاژت و .. میباشد.
مارکرهای بیوشیمیایی استخوان از نظر منشا تولید، به دوگروه اصلی تقسیم میشوند:
1ـ آنزیمها و پروتئینهایی که بهوسیلهی استئوبلاستها و یا استئوکلاستها تولید میشوند.
2ـ موادیکه درجریان تولید و یا تخریب کلاژن تیپ I (که پروتئین اصلی سازندهی ماتریکس ارگانیک استخوان است) تشکیل میشوند.
بهلحاظ بالینی و کاربردی این مارکرها در دوگروه مارکرهای ساخت و بازجذب استخوان قرارمیگیرند که مهمترین آنها درجدول1توضیح داده شدهاست.
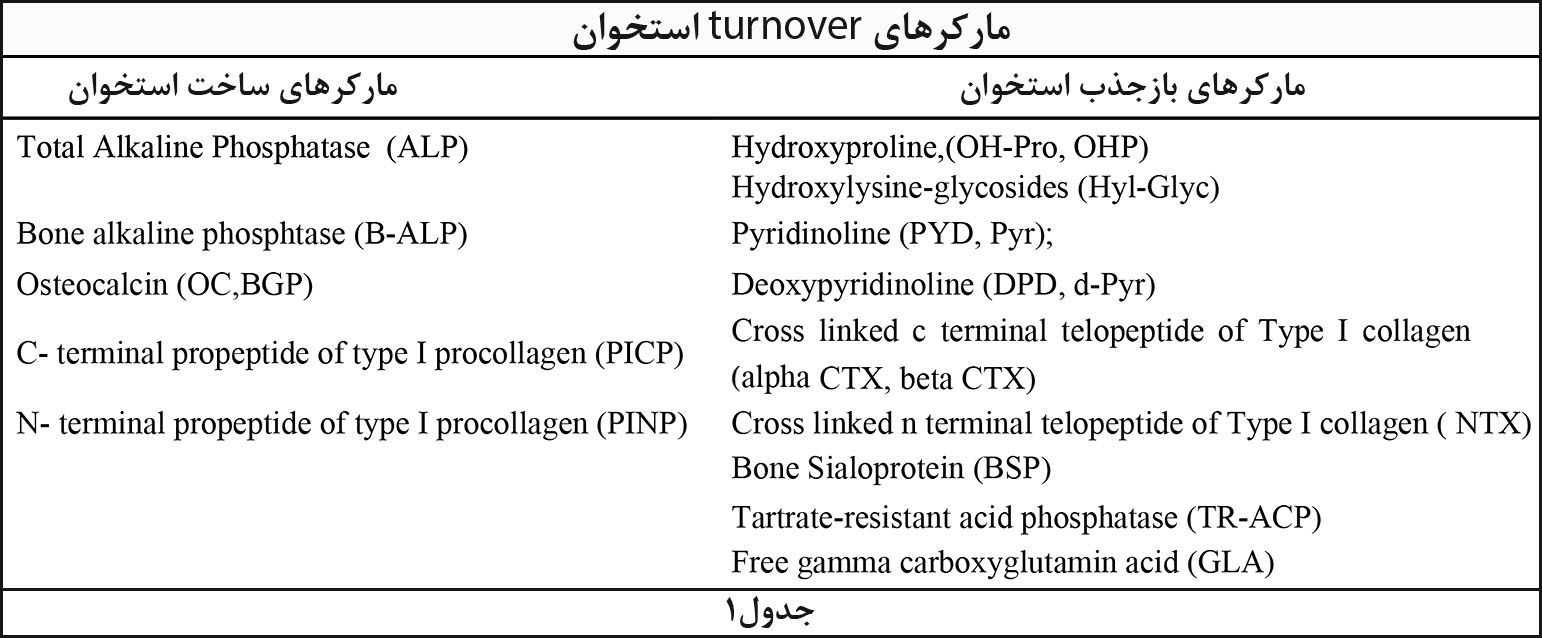
مارکرهای ساخت استخوان:
این مارکرها جنبههای مختلفی از فعالیت استئوبلاستها را نمایش داده و در سرم یا پلاسما قابل اندازهگیری میباشند.
آلکالن فسفاتاز توتال (ALP) و استخوانی (B-ALP)
ALP یک آنزیم متصل به مامبران است که به گلیکوزیل فسفاتیدیل اینوزیتول قرارگرفته روی سطح خارجی سلولها، میچسبد. بهرغم اینکه عملکرد واقعی این آنزیم مشخص نیست ولی نقش مهمی درتشکیل استئوئید و مینرالیزه شدن ایفا میکند. ALP از ایزومرهای مختلفی تشکیل شده که از کبد، استخوان، روده، طحال، کلیه و پلاسنتا منشا میگیرند. در افرادی که عملکرد کبد مناسب دارند، تقریبا50% آلکالن فسفاتاز از کبد و مابقی از استخوان منشا میگیرد. در کودکان و نوجوانان بهعلت رشد اسکلتال، آلکالن فسفاتاز استخوانی غالب بوده و تا90% آلکالن فسفاتاز تام را تشکیل میدهد.
آلکالن فسفاتاز تام خود بهتنهایی میتواند بهعنوان مارکر ساخت استخوان شناخته شود ولی فرم استخوانی شاخص اختصاصیتری برای ساخت استخوان است. برای اندازهگیری آلکالن فسفاتاز استخوانی انواع روشها ازجمله ایمونواسی طراحی شدهاست اما باید درنظر داشت درصورت افزایش فرم کبدی ممکناست بهعلت تداخل، B-ALP نیز بهطور کاذب بیش از مقـدار واقعـی بهدست آید.
استئوکلسین
استئوکلسین 15%پروتئین غیرکلاژنی درماتریکساستخوان را تشکیلداده و بهعنوان شاخص فعالیت استئوبلاست در نظر گرفته میشود. استئوکلسین دارای سه بخش گاماکربوکسیگلوتامیک اسید(Gla) وابسته به ویتامین K است که مسوول قابلیت اتصال به کلسیم این پروتئین میباشد. مقدار کمیاز استئوکلسین وارد سیرکولاسیون میشود که باتشکیل استخوان ارتباط دارد.
استئوکلسین در سیرکولاسیون عمرنیمهی کوتاهی داشته و بهسرعت توسط کلیه تصفیه میگردد بنابراین در نارسایی کلیه افزایش استئوکلسین مشاهده میگردد. این پروتئین در سرم بهسرعت تخریب شده و لذا در سرم، انواع سالم و قطعات آن بهطور همزمان دیدهمیشوند. برای سنجش استئوکلسین روشهای ایمونواسی طراحی گردیده که میتوانند فرم سالـم (1ـ49) و یـا فـــرم تخـریبشده غالب 1ـ43 (N-terminal / mid-molecule) را اندازهگیری نمایند. بهرغم اینکه اینپیشرفت درطراحی کیتهای ایمونواسی، توانسته مشکلات سنجشهای آزمایشگاهی ناشیاز تخریب سریع استئوکلسین را تاحدی کاهشدهد، همچنان پیشنهادمیگردد پساز نمونهگیری، نمونهی سرمی بهسرعت جدا شده و دردمای ۲۵- قرار گیرد.
پروپپتیدهای تایپ I کلاژن (PINP و PICP)
کلاژن تایپ I در استخوان، کلاژن غالب بوده و بهوسیلهی استئوبلاستها و به شکل پروکلاژن سنتز میگردد. پروکلاژن دارای دوگسترهیپروپپتیدN ترمینال PINP و پروپپتیدC ترمینالPICP میباشد. بعداز ترشح بهفضای اکستراسلولار ، این پروپپتیدها بهروش آنزیمی جدا شده و بهداخل سیرکولاسیون ترشح میشوند.PINP و PICP هردو ازکلاژنهای تازه ساختهشده، آزاد میشوند و لذا وجود آنها نشانهی سـاخت اخیر کلاژنI است. اگرچه این پروپپتیدها از بافتهای دیگر نیز آزاد میشوند ولی بهعلت turnover بیشتر استخوان، بخش عمدهی آنها درسیرکولاسیون از استخوان منشا گرفته است. هردو پروپپتیدهای ذکر شده در سرم و در شرایط دمایی مختلف، نسبتاً پایدار بوده و بهوسیلهی روشهای ایمونواسی قابل سنجش هستند. لازم بهذکر استPINP از ارزش تشخیصی بیشتری برخوردار است.
مارکرهای بازجذب استخوان
بهجز برخی مارکرها مانند اسیدفسفاتاز مقاوم به تارتارات، BSP و آنزیمهای مشتقاز استئوکلاستها، عمده مارکرهای بازجذب استخوان، محصولات تخریب کلاژن استخوان هستند.
هیدروکسی پرولینOHP
هیدروکــسیپرولیــن در درون سلول و از هیدروکسیلاسیون پرولیــن بهدست میآیـــد و ۱۲تا۱۴درصد اسیدهای آمینهی کلاژن بالغ را تشکیل میدهد. 90% هیدروکسی پرولین ناشی از تخریب کلاژن پس از متابولیزه شدن در کبد از طریق ادرار دفع گردیده و به روش HPLC قابل سنجش است. هیدروکسی پرولین ادرار اغلب نشانگر بازجذب استخوان است ولی باتوجه به آزادشدن از بافتهای متعـددی غیــر از استخوان، بهعنوان یکعامل غیراختصاصی شناخته میشود.
هیدروکسیلیزین ـ گلیکوزید
هیدروکسیلیزین ـگلیکوزید درجریان فاز پساز ترجمهی ساخت کلاژن ایجاد و بهدو شکل گلیکوزیل گالاکتوزیل هیدروکسیلیزین GGHL وگالاکتوزیل هیدروکسیلیزین GHL مشاهده میشود. GGHL و GHL در زمان تخریب کلاژن وارد سیرکولاسیون شده و در ادرار بهروش HPLC قابل سنجش هستند. از آنجائیکه این مارکرها بدون متابولیزه شدن دفع میشوند و تحتتأثیر رژیمغذایی قرار نمیگیرند، نسبتبه OHP برتری دارند. باتوجه به آزادشدن GGHL از سایر بافتها، GHL بهعنوان شاخص اختصاصیتری برای بازجذب استخوان شناخته میشود.
پیــریــدینـولیـــن PYD و دئوکسی پیــریــدینــولیـن
(DPD (hydroxypyridinium cross links of collagen
پیریدینولین PYD و دئوکسی پیریدینولین DPD در جریان بلوغ خارج سلولی کلاژن فیبریلار بهوجود میآیند. درزمان بازجذب استخوان، بهطریق پروتئولیز آزادشده و وارد سیرکولاسیون و نیز ادرار میشوند. باتوجه بهاینکه این مارکرها درکلاژن بالغ وجود دارند، بالارفتن غلظت آنها در خون بهمعنی تخریب کلاژن بالغ و نه کلاژن جوان است. PYD در غضروف و بافت نرم نیز یافت میشود ولی DPD در استخوان و دنتین وجود دارد و نسبت به PYD، مارکر اختصاصی تری برای بازجذب استخوان است. برای اندازهگیری PYD و DPD روشهای HPLC و ایمونواسی طراحی شده است.
تلوپپتیدهای Crosslinked تایپ I کلاژن
تلوپپتید crosslinked تایپ I کلاژن از بخشهای آمینوترمینال و کربوکسی ترمینال منشا گرفته و بهترتیب NTX و CTX خوانده میشوند. از آنجایـیکه کلاژن تایپI بیشاز90% ماتریکس ارگانیک استخوان را تشکیل میدهد، اندازهگیری انواعcrosslainked بهعنوان مارکر اختصاصی برای بازجذب استخوان شناخته میشود CTX به دو شکل آلفا در ادرار و بتا در ادرار و خون قابلسنجش میباشد. برای اندازهگیریNTX وCTX ازروشهای ایمونواسی استفاده میشود.
سیالوپروتئین استخوانی (Bone Sialoprotein(BSP
BSP یک گلیکوپروتئین فسفریله است که 5 تا10 درصد پروتئین غیرکلاژنی استخوان را تشکیل میدهد. این پروتئین محصول استئوبلاستها و ادونتوبلاستها بوده و در سرم بخش عمدهی آن متـصل بـه فاکتورH است که خود یک فاکتور اصلی تنظیمکننده در مسیر کمپلمان است. روشهای ایمونواسی موجود بخش کوچکی از BSP دردسترس را اندازهگیری میکنند. با توجه به اینکه BSP بهدنبال درمان وریدی با بیسفسفونات بهسرعت کاهشمییابد، بهعنوان مارکر بازجذب استخـوان درنظر گرفتـه میشـود.
اسیدفسفاتاز مقـاوم به تارتارات (Tartrate-Resistant Acid Phosphatase (TRAP, TRAcP
این آنزیم بخشیاز خانواده اسیدفسفاتازها است که حداقل 5ایزوفرم دیگر آن شناخته شده است. این ایزوفرمها از بافتهای مختلف مانند پروستات، استخوان، طحال، پلاکتها، اریتروسیتها و ماکروفاژها آزاد میشوند. همهی انواع اسیدفسفاتاز با ال تارتارات مهارمیشوند بهاستثنای باند 5 که بههمین علت مقاوم به تارتارات خوانده میشود. این ایزوفرم خود دارای دو ساب فرم 5a و5b میباشد که فرم5b از استئوکلاستها ترشح میشود. اسیدفسفاتاز مقاوم به تارتارات با روشهای کالریمتری قابل سنجش است ولی درزمان نمونهگیری باید توجهداشت که 20% از فعالیت آن در هرساعت در خون تام در دمای اتاق کاهش مییابد. این موضوع با اضافه کردن سیترات بافر بهنمونهی قابــلکنترل میبـاشد.
کاتپسیـنK Cathepsin) K)
کاتپسینK یکیاز اعضای خانوادهی سیستین پروتئاز است که میتواند بخش هلیکال و تلوپپتید کلاژنI را بشکند. این آنزیم در وزیکولها وگرانولها و واکوئلها در درون سیتوپلاسم استئوکلاست قرارگرفته و پساز ترشح بهداخل لاکونای بازجذب استخوان، باعث تخریب کلاژن میگردد. با توجه به اینکه کاتپسین K از استئوکلاستها و درجریان بازجذب فعال استخوان آزاد میشود، بهعنوان شاخص اختصاصی فعالیت استئوکلاستها شناخته میشود. برای اندازهگیری کاتپسین K روشهای ایمــونواسی طراحی شده است.
عوامل موثر بر مارکرهای استخوانی
بهرغم اینکه مارکرهای استخوانی میتوانند نشانگر وضعیت سیستم اسکلتی باشند و یا در بررسی پاسخ به درمان با داروهای مهارکنندهی بازجذب استخوان مورد استفاده قرار گیرند، در اندازهگیری آنها و تفسیر نتایج باید در نظر داشت که اغلب این مارکرها، تغییرات بیولوژیک درون فردی قابلتوجهی دارند و عوامل پرآنالیتیک متعددی روی نتیجهی آنها موثر هستند که موارد عمده آنها عبارتند از:
تغییرات بیولوژیک: سن، جنس، نژاد، شکستگی اخیر، حاملگی/شیردهی، مصرف داروها (مانند مهارکنندههای بازجذب استخوان، مواد آنابولیک، داروهای ضدتشنج، OCP، ...)، بیماریهای غیر اسکلتی (مانند دیابت، بیماریهای تیروئید، نارسایی کلیه، بیماریهای کبدی، بیماریهای التهابی سیستمی، بیماریهای دژنراتیو مفصل و ...)، بیتحرکی، رژیمغذایی، ورزش، تغییرات موقتی (ریتم سیرکادین، قاعدگی، تغییرات فصلی).
متغیرهای تکنیکال: نمونه و طرز نمونهگیری، نحوهی آمادهسازی و نگهدارینمونه، تخریبدمایی، تخریب در اثر نور، زمان نمونهگیری، اختلاف در نتایج حاصل از روشها و کیتهای متـفاوت.
ثبت نظر


نظرات
فروغ ملک
9 سال و 3 ماه و 16 روز پیش
ارسال پاسخ
سلام وخسته نباشید ببخشید اگه امکان داره اطلاعات کاملی درباره استئوکلسین ومکانیزم عمل ان میخواستم واینکه ایا انجمن پوکی استخوان در شیراز هست ودر صورت بودن چگونه میتوان با ان مرکز ارتباط برقرار کرد ؟با سپاس فراوان
ناشناس
9 سال و 3 ماه و 8 روز پیش
ارسال پاسخ
در هر شهر دارای دانشکده پزشکی(دانشگاه علوم پزشکی) بخش روماتولوژی وجود دارد که این انجمن مورد نظر شما درواقع بخشی از انجمن روماتولوژی آن شهر میباشد که در شیراز نیز این انجمن وجود دارد و فعال است. در شیراز به بیمارستان نمازی- بخش روماتولوژی بیمارستان مراجعه نمایید و از آقای دکتر رجایی که از پیشکسوتان روماتولوژی در شهر شیراز می باشند نیز میتوانید جویا شوید. درمورد داروی osteocalcin در سایت های wikipedia و drugs اطلاعات کاملی وجود دارد.