
99-248
عوارض نورولوژیک کووید-19
منبع :شمارۀ 1240 نشریه پزشکی امروز
اختلال عملکرد بویایی یک نشانۀ مشخص وکلیدی از عفونت COVID-19 است (بیشتر در موارد خفیف و به ویژه در افراد جوان و زنان بیشتر است). سردرد نیز از جمله الگوهایی است که رخ میدهد. درد عضلانی هم در موارد خفیف و هم در موارد شدید شایع است و در بیماران با بیشترین خطر ، با افزایش سطح CK و با آسیب احتمالی میوپاتی همراه است.
عفونت شدید ویروسیکرونا (SARS-Cov-2) مرتبط با سندرم تنفسی حاد، ممکن است منجر به ایجاد نشانههای نورولوژیک از طریق عملکرد و مکانیسمهای مختلف گردد. اگرچه عفونت مستقیم سیستمعصبیمرکزی(CNS) بسیار نادر است ، در عین حال عوارض شبهعفونی (Para-Infectous) ،برای نمونه نوروپاتیهای التهابی نیز نادر است ، روانآشفتگی(Delirium) و انسفالوپاتی سپتیک(septic encephalopathy) در بیماران دچار بیماری حاد ، شایع است. اختلال عملکرد بویایی و سردرد در موارد خفیف ، به ویژه در افراد جوان و زنان بسیار شایع است. دردهای عضلانی در موارد خفیف و حاد نیز شایع است و در بیمارانی که بیشتر در معرضخطر هستند ، با افزایش سطح کراتینکیناز (creatine kinase) و با آسیب احتمالی میوپاتی همراه است. مواردی نیز از سکته مغزی ایسکمیک (Ischemic stroke) به عنوان یک عارضه احتمالی ناشی از افزایش انعقاد خون (hypercoagulability) در ارتباط با عفونت شدید SARS-Cov-2 گزارش شده است ، اما مطالعات بیشتر مورد نیاز است. در این مقاله با عنوان "عوارض نورولوژیک کووید-19" به بررسی و ارزیابی با هدف جمع بندی یافتههای اولیه در مورد ویژگیهای نورولوژیک COVID-19 و رویکردهای درمانی آنها پرداخته شد که در ادامه ارائه خواهد شد.
▪ عوارض نورولوژیک کووید-19 :
بیشتر تظاهرات عصبی ممکن است در اوایل بیماری رخ دهد. اما به هرحال تا زمانی که مطالعات پیرامون واکسن تاثیر خود را نشان نداده و در دسترس نباشد، پژوهشهای عصب شناسی یکسان نخواهد بود. از زمان نخستین مطالعهای(نخستین مطالعه گذشتهنگر که روی بیماران حاد) که در ووهان انجام پذیرفت ، چندین نشانه عصبی به عنوان بخشی از طیف COVID-19 شناسایی شد. نشانهها شامل درد عضلانی (11٪) ، گیجی (9٪) و سردرد (8٪) بودند.
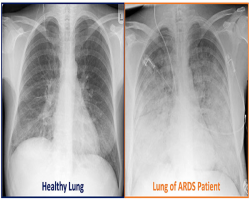
عمدهترین تظاهرات بالینی عفونت SARS-Cov-2 ناشی از عوارض ریوی است. اگرچه بیشتر نشانههای خفیف عبارتند از تب ، سردرد ، سرفه ، تنگی نفس ، دردهای عضلانی (myalgia) و فقدان حس بویایی (anosmia) است و در برخی از آنها سندروم حاد تنفسی (ARDS) نیز ایجاد میشود که ممکن است حتی منجر به مرگ شود.
پژوهشی روی 113 بیمار چینی فوت شده به دلیل ابتلا به COVID-19 (در مقایسه با بیمارانی که در نهایت زنده مانده بودند) نشان داد که ARDS با نارسایی تنفسی ، سپسیس ، آسیب قلبی حاد با نارسایی قلبی (acute cardiac injury with heart failure) و در آخر انسفالوپاتی هیپوکسیک (hypoxic encephalopathy) شایعترین عوارض بحرانی و وخیم هستند. متوسط سن بیماران فوت شده 68 سال بود و جنسیت مرد (73٪) غالب بود. فشار خون بالا و سایر بیماریهای قلبی عروقی در میان بیماران فوت شده بیشتر بود. همانطور که انتظار می رفت ، تنگینفس (dyspnoea) ، تنگی قفسه سینه ، تغییر هوشیاری ، و همچنین افزایش سطح کراتین کیناز (CK) در بیماران فوت شده به وفور مشاهده میشد.
گزارشی از نفوذ ویروسی در ساقه مغز (Brainstem-ساقه مغز بخشی از دستگاه عصبی مرکزی و در قسمت پایینی مغز قرار دارد و متشکل از بخشهاییاست که طناب نخاعی را به نیمکرههای مخ و مخچه پیوند میدهد.) در تعداد محدودی از نمونههای پاتولوژیک (از بیماران آلوده به ویروس های کرونا به غیر از SARS-Cov-2) پژوهشگران را در مورد ویژگیهای عصبی عفونتهای SARS-Cov-2 و بالقوه تهاجم عصبی مستقیم آگاه ساخت. با این حال ، تا به امروز ، این فرضیه تأیید نشده است و ارتباط آن هنوز باید ارزیابی شود.
با توجه به موارد گذشتهنگر در ووهان روی 214 بیمار بستری در بیمارستان ناشی از عفونت SARS-Cov-2 (در 41٪ از آنها شدید) نشان داد که 78 بیمار (36٪) دارای برخی ویژگیهای نورولوژیک هستند. به عنوان نمونه ، "سرگیجه" (dizziness - که بیشتر تعریف نشده است) در 17٪ موارد وجود داشت. بیماران دچار بیماری شدید و حاد، نشانههای نقصعصبی(neurological impairment) مانند آسیبهای اسکلتی عضلانی (19٪) ، اختلال هوشیاری (15٪) بیماریهای عروق مغزی (6٪) داشتند.

1. عوارض حس چشایی و بویایی در بیماری کووید -19 :
▪ اختلالات بویایی و چشایی در کوید-19 : (در موارد خفیف شایع است)
پژوهشی روی 417 بیمار مبتلا به کووید-19 (خفیف و متوسط) نشان داد که 86 و 88 درصد بیماران به ترتیب اختلالات بویایی و چشایی را گزارش کردهاند. نکته جالب اینجاست که زنان به طور قابل توجهی تحت تأثیر اختلالات بویایی و چشایی قرار داشتند. در این مطالعه ، اختلال بویایی و چشایی نسبت به نشانههای شایعتر مانند سرفه ، میالژی (حدود 58درصد) ، از دست دادن اشتها ، اسهال ، تب ، سردرد (حدود 45 درصد) و ضعف (asthenia) بیشتر بود. اختلال عملکرد بویایی پس از رفع سایر نشانهها در 63٪ موارد ادامه داشت. در میان بیمارانی که اختلال حس چشایی(anosmia) را گزارش کردند ، عملکرد بویایی در طی 2 هفته اول پس از رفع بیماری در بیش از 95٪ موارد بهبود یافت. بسیاری از ویروسها ممکن است منجر به اختلال عملکرد بویایی از طریق واکنش التهابی مخاط بینی و ایجاد رینوره (rhinorrhea) شوند که معروفترین این عوامل راینوویروس(rhinovirus) ، پاراآنفلوانزا (parainfluenza)،ویروس اپشتین-بار (Epstein–Barr virus) و برخی از سایر ویروسهایکرونا است. با این حال ، اختلال عملکرد بویایی ناشی از عفونت کووید-19 با توجه به ویژگیهای خاص خود ، به نظر می رسد با رینوره (rhinorrhea) ارتباطی ندارد.
در یک بررسی بزرگ و چند بعدی و آیندهنگر دیگری در اروپا که روی بیماران مبتلا به کووید-19 خفیف انجام شد ، میزان بالای از دست دادن حس بویایی (70٪) و اختلال عملکرد چشایی (54٪) را تأیید کرد. جوانان در مقایسه با افراد مسن بیشتر به طور مکرر از دست دادن بویایی گزارش نمودند که در زنان نسبت به مردان شیوع بیشتری دارد.
موضوع قابل اشاره،وجود شواهد بالینی در میزان شیوع اختلالات بویایی وچشایی در میان بیماران مبتلا به کووید-19 (39٪) نسبت به بیماران آنفلوآنزا (13٪) به طور قابل توجهی بیشتر بود. آنها اغلب یک آغاز شدید و حاد داشتند و تظاهرات اولیه را به همراه داشتند. انسداد همزمان بینی در بیماران کووید-19 نادر بود.نکته قابل توجه ، مشاهدۀ تورم پیاز بویایی دو طرفه ناپایدار (transient bilateral olfactory bulbs edema) در تصاویر (MRI)، بیمار مبتلا به اختلال بویایی مرتبط با COVID-19 بود.
پژوهشگران معتقدند که اپیتلیومبویایی (olfactory epithelium) ممکن است محل همانندسازی(تکثیر) و تجمع فعال SARS-Cov-2 باشد ، با توجه به اینکه سلولهای واقع شده در آن گیرندههای مورد نیاز برای عفونت SARS-Cov-2 را بیان میکنند.
اما روشهای درمانی مبتنی برشواهد محدودی برای درمان آنوسمی وجود دارد . با این حال ، اختلالات عملکرد بویایی و چشایی در بیشتر بیماران مبتلا به COVID-19 به درمانهای خاصی نیاز ندارند.
2. انواع در دردها در بیماری کووید-19 :
▪ سردرد در بیماری کرونا (در موارد خفیف شایع است) :
در یک متاآنالیز که شامل 61 مطالعه (59.254 بیمار) بود، آمار حاکی از وجود سردرد در 12٪ موارد بود، که نشان دهنده پنجمین عارضۀ بالینی در بیماری کووید-19 است (بعد از تب ، سرفه ، درد عضلانی و / یا خستگی ، تنگی نفس) .موارد گزارش شده در ووهان چین نیز تقریبا به همین میزان (13درصد) شیوع سردرد بود. اما در اروپا موضوع تفاوت داشت و طی یک بررسی صورت گرفته روی بیماران مبتلا به COVID-19 خفیف ، حاکی از شیوع بالاتر سردرد را داشت(70٪).
جوانان در مقایسه با افراد مسن بیشتر دچار سردرد میگشتند. علاوه بر این ، در زنان نسبت به مردان شیوع بیشتری وجود داشت. ماهیت مطالعه و این واقعیت که این بررسی روی بیماران با کووید-19 خفیفتر و جوانتر (میانگین سنی 39 سال) انجام شده است ، توضیحات احتمالی این درصد متفاوت با سایر پژوهشها را میدهد.
انواع گوناگونی از سردرد میتواند در طی بیماری COVID-19 ظاهر شود. پژوهشگران معتقدند که سردرد از روز هفتم پس از شروع نشانههای بالینی مربوط به کووید-19، میتواند ناشی از طوفانسیتوکینی(cytokine storm) مرتبط با عفونت باشد که همچنان نیاز به پژوهشها بیشتر دارد.
از آنجا که هیچ گزینه درمانی خاصی برای سردرد مربوط به کووید-19 گزارش نشده است ، مدیریت درد (Pain Management) توصیهای است که توسط پزشکان و متخصصان میشود.

3. عوارض سیستم عصبی مرکزی در بیماری کووید-19:
▪ عوارض اختلالهوشیاریو روانآشفتگی ناشی از کرونا (که در موارد حاد، شایع است) :
پژوهشگران و پزشکان طی گزارشی اعلام نمودند که روند تغییر هوشیاری (altered consciousness) هنگام پذیرش در بیمارستان، بیشتر در بیمارانی بوده که متعاقب آن فوت کردهاند (22٪) و در افرادی که سرانجام از بیماری بهبود یافتند (1٪) بود.
در بررسی دیگری که روی ویژگیهای نورولوژیک 58 بیمار مبتلا به سندرمدیسترسحاد تنفسی (ARDS) ناشی از کووید-19 متمرکز بود ، آژیتاسیون یا سراسیمگی یا بیقراریروانی (Agitation) در 40 بیمار (69%) هنگامی که انسداد عصبی عضلانی(Neuromuscular Blockade) متوقف شد، مشاهده گردید که به احتمال زیاد با دلیریوم هایپرکینتیک (hyperkinetic delirium) مرتبط است .در ادامه 33 درصد بیمارانی که از بیمارستان ترخیص شدند ، دچار سندروم بدعملکردی ( Dysexecutive Syndrome) بودند که متشکل از بیتوجهی ، ناآگاهی (disorientation)، و واکنش ضعیف حرکتی در برابر دستور (poorly organized movements in response to command) بود.
در بیمارانی که تحت پونکسیون نخاعی (Lumbar puncture) جهت بررسی SARS-Cov-2 قرار گرفتند ، نمونههای مایع مغزی نخاعی (CSF) در هفت بیمار منفی بود . الکتروانسفالوگرافی (EEG) و MRI مغز، یافتههای غیر اختصاصی را نشان داد (فقط دو بیمار اندکی سکته مغزی ایسکمیک حاد (small acute ischemic stroke) داشتند). اما مطالعات و بررسیهایی نیاز است تا مشخص گردد که از عوارض انسفالوپاتیکی که در طی بیماری رخ میدهد ناشی از عفونت SARS-Cov-2 بوده یا به دلیل شرایط حاد مرتبط با انسفالوپاتی، سیتوکینها و / یا داروها میباشد.
بررسیها در ووهان همچنین نشان داد که تظاهرات سیستم عصبی، در عفونتهای حاد ناشی از SARS-Cov-2 در مقایسه با گونۀ خفیف بیشتر مشاهده گردید. برای نمونه ، "اختلال هوشیاری(impaired consciousness)" در حدود 15 درصد از افراد به شدت بیمار در مقایسه با حدود 2درصد از سایر بیماران گزارش شدهاست.
اختلال هوشیاری و روانآشفتگی با نشانههای هرمی در ارتباط هستند (Pyramidal Signs). واکنشهای افزایش یافتۀ تاندون (enhanced tendon reflexes)، کلونوس مچ پا (ankle clonus) ، رفلکسهای کف پا اکستنسور دو طرفه (bilateral extensor plantar reflexes) که در 67٪ بیماران مبتلا به سندرمدیسترسحاد تنفسی (ARDS) گزارش شده است.
اختلال هوشیاری و دلیریوم یا همان روانآشفتگی ناشی از COVID-19 به احتمال زیاد ناشی از انسفالوپاتی توکسیک عفونی (یا "سپتیک") میباشد که نوعی سندروم اختلال عملکرد مغز برگشت پذیر(reversible brain dysfunction syndrome) بوده و ناشی از عواملی مانند پاسخ التهابی سیستمیک (systemic inflammatory response) ، زهرخونی (Toxemia) و هیپوکسی در طی عفونت حاد ریوی (acute pulmonary infection) میباشد و نیازمند یک بررسی بسیار گسترده است.
از این رو اجرای امور مربوط به پیشگیری روانآشفتگی و مدیریت بالینی بیمار در حین همهگیری کووید-19 از اولویت برخوردار است.
مطالعهای که در حین درمان بیماران مبتلا به کووید-19 صورت پذیرفت ، نشان داد که بنزودیازپین (Benzodiazepine) در برابر آژیتاسیون پاسخ مناسب نشان میدهد . موضوع مهمی که باید بدان توجه داشت این است که ، بنزودیازپینها ممکن است برای بیماران مبتلا به نارسایی تنفسی (respiratory failure) که تحت درمان با ونتیلاتور نیستند خطرناک بوده و نیازمند مراقبت و توجه ویژه هستند.
در مواردی نیز ، روانآشفتگی هایپراکتیو (hyperactive delirium) بوده و نیازمند مدیریت تهاجمیتر باشد، که در درمان دلیریومهای ناشی از کووید-19 ، نیز باید روند درمانی استاندارد ارائه گردد.

▪ عوارض سکته مغزی ایسکمیک ناشی از کرونا (نادر):
در یک بررسی گذشتهنگر انجام گرفته در شهر ووهان ، سکتهمغزیایسکمیک در پنج نفر از بیماران مبتلا به کووید-19 از نوع حاد (حدود 5 درصد) در مقایسه با تنها یک نفر ( 1 درصد) در گروه بیماران مبتلا به کووید-19 متوسط گزارش شده است. جالب اینجاست که بیماران مبتلا به عفونت شدید، سطح D-dimer بالاتری داشتند که نشان دهنده سیستم انعقادی تحلیل رفته (consumptive coagulation system) است. متأسفانه ، در این بررسی رابطه میان سکته مغزی و سطح D-dimer ارائه نشده است.
در یک بررسی انجام شده در کشور هلند،ارزیابی روی 184 بیمار بستری در ICU و دچار ذاتالریه ناشی از کووید-19 انجام گرفت که عوارض ترومبوتیک بالینی زیر مشاهده گردید :
حدود 14 درصد ترومبوآمبولی ریوی ، حدود 2 درصد حوادث گوناگون ترومبوامبولیک وریدی و حدود 2 درصد نیز سکته ایسکمیک مغزی .
در بررسی دیگری که در شهر میلان ایتالیا صورت پذیرفت ، همین میزان سکته مغزی گزارش شد(2.5 درصد) . سه نفر از آنها در ICU و شش نفر در بخش عمومی بودند که در 6 نفر آنها دلیل اصلی بستری سکتۀ مغزی بود. در آمریکا نیز نزدیک 1.1 درصد از بیماران بستری شده به دلیل کووید-19 نیز گزارش سکته مغزی ایسکمیک را داشتند.
علاوه بر این ، یک زن 36 ساله اسپانیایی دچار سکته در ناحیۀ شریان مغزی میانی سمت چپ که بر اثر وجود لختهای شناور و آزاد در آئورت صعودی، نیز در حین ابتلا به عفونت SARS-Cov-2 گزارش شده است.
زنجیرهای از موارد نیز در لندن گزارش شد که طی آن ، شش بیمار پیاپی را با سکته مغزی ایسکمیک حاد و COVID-19 گزارش نمود. هر شش بیمار انسداد رگ بزرگ با سطح D-dimer قابل توجهی افزایش یافته (≥μg/L 1000) داشتند. پنج نفر از این بیماران، لوپوس آنتی کوآگولانت مثبت (positive lupus anticoagulant) داشتند ( اما ارتباط بیماریزایی آنها قطعی نیست).
سه بیمار دارای انفارکتوس چند سطحی (multiterritory infarcts) بودند ، دو نفر ترومبوز وریدی همزمان(concurrent venous thrombosis) داشتند و در دو مورد سکتههای ایسکمیک علی رغم تجویز داروهای ضد انعقادی رخ داد.
الگوهای پیش انعقادی (procoagulant) بیماران مبتلا به کووید-19 گزارشهای بالینی عوارض ترومبوآمبولیک ، از جمله سکته مغزی ، را در طول بیماری توجیه میکند.
بیماران مبتلا به سندرمدیسترسحاد تنفسی (ARDS) ناشی از کووید-19 یک نمایۀ انعقادی را نشان میدهند که با افزایش قدرت لخته مشخص میگردد که به دلیل سهم پلاکت و فیبرینوژن ، افزایش سطح D-dimer و hyperfibrinogenemia (احتمالاً به افزایش اینترلوکین -6 ، یک سیتوکین ضد التهاب قدرتمند مرتبط است) میباشد. در شدیدترین موارد ممکن است حداقل یک درمان ضد ترومبوتیک تهاجمی توجیه پذیر باشد (به عنوان نمونه هپارین با وزن مولکولی کم 6000 IU ، دو بار در روز) همچنین برای ارزیابی بهترین پیشگیری و درمان این بیماری ، به مطالعات بیشتری نیاز است. در همین راستا مطالعاتی در حال انجام است که طی آن یک آزمایش کنترل شده تصادفی در حال برنامه ریزی است که آیا دوز پیشگیریکنندۀ (prophylactic-dose) انوکساپارین (در مقابل عدم درمان) ممکن است سبب کاهش مرگ و میر زودرس و بستری شدن برنامه ریزی نشده در بیماران مبتلا به COVID-19 که هیچ اندیکاسیون دیگری برای دریافت ضد انعقاد ندارند ، میگردد یا خیر ؟
مطالعه دیگری تأیید کنندۀ این موضوع بود که اختلال عملکرد انعقاد خون (coagulation dysfunction) در بیماران مبتلا به COVID-19 ، به ویژه افزایش فیبرینوژن و D-dimer ، شایع است و میزان افزایش آن به شدت بیماری مربوط است. با بهبودی بیمار ، فیبرینوژن و زمان ترومبوپلاستین جزئی فعال (activated partial thromboplastin time ) نیز به حالت طبیعی باز میگردد.
با این حال ، موضوع سکتهمغزی در عفونتهای SARS-Cov-2 همچنان مورد بحث است. به عنوان نمونه ، هیچ افزایش قابل توجهی در بروز سکته مغزی طی بیماری COVID-19 در برخی از مناطق آسیب دیده ، برای نمونه در بخشهای شمالی کشور ایتالیا مشاهده نشده است.

▪ عوارض نادر سیستم عصبی مرکزی ناشی از کرونا :
گزارشهایی از عوارض نادر مختلف عصبی طی دورۀ همهگیری در بیماران مبتلا به کووید-19 وجود دارد ، عارضههایی مانند خونریزیمغزی (intracerebral hemorrhage)،ترومبوز وریدیمغزی (cerebral venous thrombosis)، سفتیجزئیگردن (slight neck stiffness) بدون وجود هیچگونه ژنوم SARS-Cov-2 در مایع مغزی-نخاعی(CSF) ، میوکلونوس تعمیم یافته (generalized myoclonus) ، تشنج ، بحران صرعی (Status epilepticus) و آنسفالوپاتی صرعی حاد (acute epileptic encephalopathy) ، سندرم انسفالوپاتی برگشت پذیر خلفی هموراژیک (hemorrhagic posterior reversible encephalopathy syndrome) ،انسفالوپاتی نکروزان حاد (acute necrotizing encephalopathy) ، ماده سفید (White Matter) ضایعات التهابی گلوبوس پالیدوس (globus pallidum inflammatory lesions) ، لکوآنسفالوپاتی منتشر با ریزخونریزیها (diffuse leukoencephalopathy with microhemorrhages) و . . .
بر اساس ملاحظات تئوریک ، پیشنهاد شده است که هنگام کنترل بیماران مبتلا به کووید-19 با شرایط بحرانی که با تغییر وضعیت روانی روبرو هستند ، باید با کنترل مستمر EEG مطمئن شوید که صرع غیرتشنجی ادامه ندارد.
یک مطالعه گذشته نگر به طور خاص از چین ، حاکی از آن است که تشنج در طول COVID-19 موضوعی بسیار نادر است. در مجموع 304 نفر مورد مطالعه قرار گرفتند که از این تعداد 108 نفر وضعیت بحرانی و سختی داشتند. در طول بستری شدن فقط دو نفر نشانههای تشنج مانند داشتند. بنابراین ، هیچ مدرکی مبنی بر وجود خطر تشنج در افراد مبتلا به COVID-19 وجود نداشت.
هنگام درمان صرع در بیمار مبتلا ، مهم است که تداخلات دارویی داروهای ضدصرع و داروهای مورد استفاده در درمان COVID-19 در آن فرد بررسی شود.
توجه ویژهای برای کاربامازپین(carbamazepine) ، فنیتوئین(phenytoin) ، فنوباربیتال(phenobarbital) و پریمیدون(primidone) لازم است. فهرست بهروز شدهای توسط دانشگاه لیورپول منتشر شده در اینجا موجود است:
www.covid19-druginteractions.org
3. عوارض ماهیچهای و عصبی در بیماری کووید-19:
▪ درگیری و دردهای عضلانی ناشی از کرونا (شایع):
در مطالعات انجام گرفته در اروپا که روی بیماران مبتلا به کووید-19 خفیف انجام شد ، شیوع بالای درد عضلانی را در این بیماران گزارش کرد (63٪). در مقابل ، یک مطالعه بزرگ و آیندهنگر از نیویورک روی بیماران مبتلا به کووید-19 حاد گزارش نمود که درد عضلانی در 26٪ این بیماران وجود دارد.
در یک مطالعهای که در چین روی بیماران بدحال انجام گرفت ، درد عضلانی را به عنوان یک نشانۀ آغاز بیمار در 22٪ از بیماران گزارش کرد. سطح متوسط CK (مقادیر طبیعی کمتر از 190) در بیمارانی که متعاقباً فوت کردند (U / L 189) نسبت به سایر بیماران (U / L 84) بالاتر بود.
مطالعه دیگری از ووهان چین گزارش مشابهی را منتشر نمود:
آسیب عضلانی اسکلتی (به روش زیر تعریف شده است: هنگامی که بیمار دچار درد عضلانی اسکلتی و افزایش سرم CK ، بیش از 200 U / L میگردد) به طور قابل توجهی در عفونتهای شدید، در مقایسه با عفونتهای خفیفتر (19 در مقابل 5٪) شایعتر بود.
سطح متوسط CK در گروه شدید بالاتر بود: U/L 83 (محدوده12.216-9) در مقایسه با U/ L 59 (1260 -19). نکته قابل توجه ، بیماران با آسیب عضلانی ، درعین حال دچار آسیب چند عضوی نیز هستند ، از جمله ناهنجاریهای جدی در کبد و کلیه. رابدومیولیز (Rhabdomyolysis) شدید ممکن است یک عارضه نادر باشد که با COVID-19 همراه است.
حتی اگر الکترومیوگرافی ، تصویربرداری از عضله یا هیستوپاتولوژی عضله در دسترس نباشد ، بر اساس دادههای موجود ، عفونتهای ویروس کرونا ممکن است سبب میوزیت ویروسی شود.

▪ نوروپاتیهای التهابی نادر ناشی از کرونا :
تعدادی گزارش نیز از بیمارانی ارائه شده که در طی یا بعد از بیماری COVID-19 ، پلی نوروپاتی دمیلینه کننده التهابی حاد (acute inflammatory demyelinating polyneuropathy) را تجربه نمودند.
یک مورد نیز پلی رادیکولونوریت حاد (acute polyradiculoneuritis) با سندرم قفلشدگی(Locked-in syndrome) در بیمار مبتلا به COVID-19 نیز گزارش شد. در طی این بیماری ، گزارشی از یک مورد نوروپاتی آکسونال حرکتی حسی حاد (Acute Motor Sensory Axonal Neuropathy) گونهای شدید از سندرم گیلن-باره گزارش شد ، اما از مایع مغزی-نخاعی (CSF) آن نمونه برداری نشد. بیشتر این بیماران تحت درمان با ایمونوگلوبولینهای وریدی (IVIg) قرار گرفتهاند که نتیجه آن متغیر است.
علاوه بر این ،در اسپانیا، مقالهای گزارش دو مورد را نشان داد که وقوع سندرم نادر میلر فیشر(Miller Fisher syndrome) و پلینوریت جمجمه (polyneuritis cranialis ) در طول بیماری همهگیر COVID-19 است.
نخستین مورد با IVIg درمان شد. دو هفته بعد ، هر دو بیمار بهبودی عصبی کامل پیدا کردند. دو بیمار پس از مراجعه برای معاینات تکمیلی تشخیص ابتلا به کووید-19 در آنها داده شد.
اما در ایتالیا گزارشهایی دقیق حاکی از آن است ،که پنج بیمار پس از تشخیص و آغاز COVID-19 به سندرم گیلنباره مبتلا بودند. چهار نفر از این بیماران در آغاز سندرم نورولوژیک خود، سواب نازوفارنکسِ آنها برای SARS-Cov-2 ، مثبت بود.
در حالی که موردِ پنجم دارای تست سرولوژی مثبت بود. از نخستین نشانههای سندرم گیلن-باره ، ضعف اندام تحتانی و خوابرفتگی (Paresthesia) در چهار بیمار و دیپلژی(Diplegia) صورت و به دنبال آن آتاکسی و اختلالات حسی در یک بیمار بود.
در چهار بیمار در طی یک دوره 36 ساعته تا 4 روزه تتراپارزی شایع یا تتراپلژی مشاهده گردید که 3 بیمار تحت تهویه مکانیکی قرار گرفتند. فاصله میان آغاز نشانههای کووید-19 و نخستین علائم سندرم گیلن باره از 5 تا 10 روز متغیر بود. در ارزیابی CSF ، دو بیمار دارای سطح پروتئین طبیعی بودند و تمام بیماران از میزان طبیعی گلبولهای سفید برخوردار بودند. آنتیبادیهای آنتی گانلیوزید (Antiganglioside antibodies) وجود نداشت. در تمامی بیماران ، ژنوم SARS-Cov-2 در CSF یافت نشد. یافتههای الکتروفیزیولوژیک با یک نوع آکسونی از سندرم گیلن-باره در سه بیمار و با یک فرآیند دمیلینه سازی در دو بیمار مطابقت داشت.
MRI افزایش ریشههای عصب انتهایی یا دُمی (caudal nerve) را در دو بیمار و عصب صورت را در یک بیمار دیگر نشان داد.
تمام بیماران با IVIg تحت درمان قرار گرفتند. دو نفر دوره دوم IVIg را دریافت کردند و یکی تعویض پلاسما(Plasma Exchange) را آغاز کردند. در 4 هفته پس از درمان ، فقط یک بیمار ترخیص شده و قادر بود به طور مستقل راه برود.
اگر یافتههای مربوط به تصویربرداری از قفسه سینه با شدت نارسایی تنفسی در بیماران کووید-19 متناسب نباشد ، باید اثر ظرفیت حیاتی کاهش یافته به دلیل نارسایی عضلانی از سندرم گیلن-باره در نظر گرفته شود.
درمان سندرم گیلن-باره مرتبط با عفونت SARS-Cov-2، با درمان نوروپاتیهای حاد التهابی دیگر تفاوتی ندارد. با این حال ، تعویض و تبادل پلاسما ممکن است سازماندهی بهتری در بیمار نسبت به تزریق IVIg ایجاد کند ، به ویژه در بیمارانی که همچنان درگیر عفونت هستند.
▪ گزارش پزشکی (Case Report) نورولوژیک طی همهگیری کووید-19 :
یک بیمار مرد در 70 سالگی با اختلالات حسی و حرکتی موقتی در سمت چپ بدن (6 ساعت) به پزشک مراجعه کرد. سابقه پزشکی وی از نظر پرفشاری خون ، دیابت نوع 2 ، نارسایی مزمن کلیوی ، دیس لیپیدمی و بیماری ایسکمیک قلب همراه با سکته قلبی قابل توجه بود. وی دارای دفیبریلاتور کاشتنی قلبی (ICD) و ضربانساز قلب (ناسازگار با MRI) بود. او سیگاری بود. وی به دلیل ذاتالریه دوطرفه ناشی از کووید-19 در بیمارستان به مدت 27 روز بستری بود و یک روز پیش از ترخیص ، RNAهای SARS-Cov-2 در نمونههای آزمایشگاهی نازوفارنکس، توسط واکنش زنجیرهای پلیمراز رونویسی معکوس قابل تشخیص بود. سیتی مغز (چپ) و angioCT (راست)، ترومبوز در شریان خلفی مغز راست (فلش) را نشان داد. هنگامی که وی تحت ارزیابی قرارگرفت ، اختلالات رفع شد و معاینه عصبی طبیعی بود. بنابراین ، هیچ معیاری برای ترومبولیز سیستمیک یا ترومبکتومی مکانیکی وجود نداشت و وی تحت درمان استاندارد پزشکی قرار گرفت.

▪ عملکرد نورولوژیک طی همهگیری کووید-19
عملکرد نورولوژیک (Neurological Practice) در طی دورۀ همهگیری تحت تاثیر کووید-19 قرار گرفت. بیماران مبتلا به اختلالات عصبی عضلانی (برای نمونه میاستنی گراویس) و بیماریهای نورودیژنراتیو (برای نمونه زوال عقل ، بیماری پارکینسون) ممکن است به صورت ویژه در معرض عفونت SARS-Cov-2 و عوارض آن باشند. باتوجه به الزام قرنطینه و خانه نشینی در دوران همهگیری ، جلسات درمانی غیر ضرور و آزمایشهای تشخیصی عصبشناختی نیز متعاقب آن لغو گردید. یک متاآنالیزجدید نشان داد که در مجموع 8 درصد از بیماران مبتلا به کووید-19 حاد ، به بیماریهای نورولوژیک دچار بودند.
علاوه بر این ، بسیاری از بیماران مبتلا به بیماریهای خود ایمنی عصبی مانند مولتیپلاسکلروزیس ، سندرم دویک (Neuromyelitis optica)، میاستنی گراویس ، نوروپاتی ها و میوپاتیهای التهابی ، تحت درمانهای سرکوب کننده سیستم ایمنی(immunosuppressive) هستند.
توصیه بر آن است که این گروه از بیماران برای پیشگیری از قرار گرفتن در معرض ویروس و ارزیابی مجدد دوزهای داروها اقدامات احتیاطی بیشتری انجام دهند.
▪ نتیجهگیری:
عفونت SARS-Cov-2 از طریق مکانیسمهای مختلف ممکن است منجر به بروز عوارض نورولوژیک شود. اگرچه عفونت مستقیم CNS بسیار نادر است و عوارض ناشی از عفونت (به عنوان مثال نوروپاتی های التهابی و احتمالاً التهاب حاد منتشره مغزی ADEM) نادر است ، اما دلیریوم و انسفالوپاتی سپتیک در بیماران دچار شرایط حاد بیمار، شایع است.
اختلال عملکرد بویایی یک نشانۀ مشخص وکلیدی از عفونت COVID-19 است (بیشتر در موارد خفیف و به ویژه در افراد جوان و زنان بیشتر است). سردرد نیز از جمله الگوهایی است که رخ میدهد. درد عضلانی هم در موارد خفیف و هم در موارد شدید شایع است و در بیماران با بیشترین خطر ، با افزایش سطح CK و با آسیب احتمالی میوپاتی همراه است. سکته مغزی ایسکمیک به عنوان عارضه احتمالی افزایش انعقاد خون در ارتباط با عفونت شدید SARS-Cov-2 گزارش شده است.
به عنوان سخن پایانی اینگونه میتوان بیان نمود که با توجه به نوظهور بودن این ویروس و عارضههای احتمالی ، مطالعات بیشتری پیرامون تاثیرات نورولوژیک بر سلامت انسان نیاز است که به طور حتم و در صورت حصول نتایج جدید تقدیم خوانندگان محترم خواهد شد.
▪ دکتر برزو سالک
مدیرعلمی نشریه پزشکی امروز
پژوهشگر و مدیرعالی و اجرایی پروژههای دانش بنیان درحوزه ویروسشناسی
▪ دکتر اکبر سلطانزاده
استاد بیماریهای مغزواعصاب دانشگاه علوم پزشکی تهران

▪ منابع :
1-Clinical characteristics of 113 deceased patients with coronavirus disease 2019: retrospective study. BMJ. 2020
2-Coronavirus diseases (COVID-19) current status and future perspectives: a narrative review. Int J Environ Res Public
Health
3-Scoping review of prevalence of neurologic comorbidities in patients hospitalized
for COVID-19. Neurology. 2020
4-Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. Lancet. 2020
5-Neurologic complications of coronavi
rus infections. Neurology. 2020
6-The neuroinvasive potential of sars-cov2 may play a role in the respiratory failure of COVID-19 patients. J Med Virol.
2020
7-Neurologic manifestations of hospitalized patients with coronavirus disease 2019 in Wuhan, China. JAMA Neurol. 2020
8-Olfactory and gustatory dysfunctions as a clinical presentation of mild-to-moderate forms of the coronavirus disease (COVID-19): a multicenter European study. Eur Arch Otorhinolaryngol. 2020
9-Clinical and epidemiological characteristics of 1,420 european patients with mild-to-moderate coronavirus disease 2019. J Intern Med. 2020
10-Acute-onset smell and taste disorders in the context of COVID-19: a pilot multicenter PCR-based case-control study. Eur J Neurol. 2020
11-New onset of loss of smell or taste in household contacts of home-isolated SARS-CoV-2-positive subjects. Eur Arch Otorhinolaryngol. 2020
12-Bilateral transient olfactory bulbs edema during COVID-19-related anosmia. Neurology. 2020
13-Sars-cov-2: olfaction, brain infection, and the urgent need for clinical samples allowing earlier virus detection. ACS Chem Neurosci. 2020
14-Anosmia-a clinical review. Chem Senses. 2017
15-Novel coronavirus infection (COVID-19) in humans: a scoping review and meta-analysis. J Clin Med. 2020
16-Headaches during COVID-19: my clinical case and review of the literature. Headache. 2020
17-Neurologic features in severe sars-cov-2 infection. N Engl J Med. 2020
18-Nervous system involvement after infection with COVID-19 and other coro
naviruses. Brain Behav Immun. 2020
19-COVID-19: ICU delirium management during sars-cov-2 pandemic. Crit Care. 2020
20-Characteristics, symptom management and outcomes of 101 patients with COVID-19 referred for hospital palliative care. J Pain Symptom Manage. 2020
21-Hyperactive delirium requires more aggressive management in patients with COVID-19: temporarily rethinking “low and slow” J Pain Symptom Manage. 2020
22-Delirium in critically ill patients. Handb Clin Neurol. 2017
23-Incidence of thrombotic complications in critically ill ICU patients with COVID-19. Thromb Res. 2020
24-Venous and arterial thromboembolic complications in COVID-19 patients admitted to an academic hospital in Milan, Italy. Thromb Res. 2020
25-COVID-19 related neuroimaging findings: a signal of thromboembolic complications and a strong prognostic marker of poor patient outcome. J Neurol Sci. 2020. Thromb Res. 2020
26-Emergency room neurology in times of COVID-19: malignant ischemic stroke and sars-cov2 infection. Eur J Neurol. 2020









ثبت نظر