عود و مقاومبودن بیماری هوچکین، مشکلی چالشبرانگیز برای پزشکانی است که بدخیمیهای خونی را درمان میکنند. درمان رایج (Standard) این بیماران باید شامل شیمیدرمانی نجاتدهنده و سپس پیوند مغز استخوان اتولوگ باشد. بخصوص در بیماری که حساس به شیمی درمانی باشد.
موضع بارز در این زمینه عبارتست از تدابیر Imaging، رژیم مخصوص شیمیدرمانی قبل از پیوند مغزاستخوان (ASCT) و رادیوتراپی استحکامی. بعضی از بیماران واجدشرایط برای پیوند مغزاستخوان نیستند و باید با شیمیدرمانیهای موجود و رادیوتراپی درمان شوند.
عوامل پیشآگهیدهندهای برای عود و یا مقاومبودن بیماری وجود دارد که باید توجه شود.
پیوند مغزاستخوان آلوژن گرچه پتانسیل اثرGraft-Versus Lympnoma دارد ولی حاوی سمیت شدید و عمر عاریاز بیماری اندکی میباشد؛ بنابراین توصیهنمیشود و این طریق درمان باید بهعهده Clinical trial گذاشته شود. داروهای جدیدی بهعنوان تک داروی مؤثر موجود و درحال وسعت گرفتن میباشد که امیدوارکننده در درمان اَشکال عود کننده و مقاوم این بیماری میباشند.
مقدمه:
درمان بیماری هوچکین با درجهی محدود، پیشرفت بسیار زیادی کردهاست. شکست درمانی دراینگروه از بیماران حدود ۱۰درصد است گرچه معالجهی بیماران با گرفتاری وسیع نیز با موفقیت همراه است ولی ۱۰درصد از آنها به خاموشی کامل (CR) نمیروند و ۲۰تا۳۰درصد از آنها که به خاموشی کامل رفتهاند، نهایتاً بعداز درمان عودمیکنند.
شیمیدرمانی نجاتدهنده (salvage) و متعاقب آن پیوند بنیاختهها، درمان انتخابی در افراد دچار به عود و یا مقاوم به دارو درمانی انتخابی است.
محققان دو بررسی (Randomized) در فاز۳ نشاندادهاند که بهبودی در پیشرفت عاریاز بیماری (PFS) با داروهای دوز بالای شیـمیدرمانی (High Dose Chemotherapy :HDCT)نسبت به درمان نجاتدهندهی معمولی (Standard) بیشتر بوده گرچه ازنظر آماری (Statistic) در طولعمر (OS) بیماران اهمیت چندانی نداشته است.
گرچـه ایــن بررسیهای تصــادفی کنتـرلشـده (Randomized Controlled Trials=RCT)، پایه و اساس درمان افراد دچار به عود و یا مقاوم به درمان میباشد ولی کاربرد آن و اطلاعات دیگر در نوشتهها (Literatura) چالشبرانگیز مانده است. ما دراینجا سعی در تمرکز روی بعضیاز مشکلات و جدل و مجادله در درمان، شامل پیشرفت بیماری و یا عدم پاسخ درمانی، تعیین عوامل پیشآگهی و استفاده از Imaging و داروهای در دسترس شامل انجام پیوند و یا پرهیز از پیوند مینمائیم.
تشخیص عود و یا مقاومبودن به درمان:
باتوجه به دسترسی به سیتیاسکن و اخیراً PET و یا CT.PET و تکرار آنها درحین و یا بعداز انجام درمان اولیه، بیشتر میتوان به میزان پاسخدرمانی و درمواردی به عود بیماری پیبرد. گاهی مثبتبودن این طریق imaging در نزد بیماریکه هیچگونه نشانهای ندارد (Asymptomatic) سبب میشود که برای پزشک معالج سئوالبرانگیز باشد.
(National comprsehensive cancer Network (NCCN درسال۲۰۱۰ بهعنوان راهنمایی توصیهکرد که ۶تا۱۲ماه بعداز اتمام درمان در Grade 2A عکس ریه و یا سیتیاسکن قفسهیصدری و در Grade 2B سیتیاسکن شکم و لگن درخواست شود. گرچه بعضیها برای این روش در نزد بیماری که در خاموشی کامل و بدون نشانه است، در کشف عود بیماری، ارزش محدودی قائل هستند.
توصیه شدهاست که باید بیوپسی بعدی در مواردی که تشخیص اولیه گنگ و نامعلوم بوده و یا بعد از بهبودی کامل لنفاونوپاتی تازه ایجاد شده باشد و یا بعداز مدت طولانی (بیشاز ۳تا۵سال) رخ داده باشد، انجام گیرد و یا پزشک حدس بزند که ممکناست بیماری دیگر درکار باشد. گرچه در بیشتر موارد که درمان دستدوم مدنظراست، رادیوگرافی پیشرفت بیماری را درحین درمان و یا زمان کوتاهی بعداز درمان نشانمیدهد لذا ما عقیده داریم روش تهاجمی و قبول خطر عارضه معقول نیست.
گرچه اطلاعات در مورد استفاده از اسکن PET متقاعدکننده نیست ولی استفاده از PDG-PET برای تعیین پاسخ درمان اولیه و مراقبت و نظارتبر بهبودی کامل بیماری، موردتأیید روزافزون قرارگرفته و آن را بعداز ۶تا ۸هفته بعداز شیمیدرمانی و ۸تا۱۲هفته بعداز رادیوتراپی توصیه مینمایند.
متأسفانه مثبتبودن آزمایش PET بهاندازهی منفیبودن آن اهمیت ندارد. چون PET مثبت کاذب در مواردی که Rebound Thymic Hyperplasia در افراد جوان انفلاماسیون موضعی بعداز شیمیدرمانی و یا رادیوتراپی سارکوئیــدوز، رسوب Brown Fat دیدهمیشود. در گزارشهای اخیر شامل۵۷بیمار با هوچکین مدیاستن، بیشتـر افرادیکه در stage 1 و یا stage 2 قرارداشتند و ۲۵فردی که Mediastinal Mass داشتند، در ۲۱تَن در آخر درمان از آنها PET مثبت گزارششده بود که در پیگیــری با بیــوپسی فقط در۱۰تَن از ۲۱بیمار عود بیماری تأییدشــد. در بـررسی در Memorial- Kettering Cance Center درمورد Diffuse Large Cell Lymphoma بعداز درمان اولیه گزارششده که درمورد PET مثبت باید خیلی احتیاطکرد چون فقط در ۵تَن از ۳۸ بیمار بیوپسیشده با PET مثبت، لنفوم وجود داشت (موارد مثبت کاذب بالا).
بررسی گروه لنفومِ هوچکین آلمان نشانداد که رادیوتراپی در محلPET مثبت، موجب بهبودی در ۸۶درصد در مقابل ۹۵درصد آنها که PET منفی داشتند گردید.
درنتیجه ما Serial Imaging را در فردیکه نشانهای ندارد (Asymptomatic) و دورههای درمانی را گذرانده است توصیهنمیکنیم و به راهنمایی NCCN (هــر۶تـا۱۲ماه Serial Imaging) نیز عقیدهنداریم چون بیمار زیربار رادیاسیون و هزینهی زیاد خواهد رفت. در عوض بیوپسی مجدد را برای تأیید پیشرفت بیماری و یا مواردیکه شک درمورد نتیجهی بیوپسی اول وجود داشته باشدیا عود بیماری بعداز مدتطولانی حدسزده شود و مخصوصاً اگر احتمال بیماری دیگری میرود، توصیه میکنیم. همچنین، بیوپسی را موقعیکه FDG-PET مثبت گزارش شدهاست و قراراست درمان نجاتبخش (Salvage) با پیوند مغزاستخوان شروعشود، توصیه مینمائیم.
عوامل پیشآگهی دهندهی جدول۱ که زمان عود برای شروع درمان، مرحلهی پیشرفتهی بیماری درموقع عود و حال عمومی بد نشانمیدهد را نیز باید درنظرگرفت.
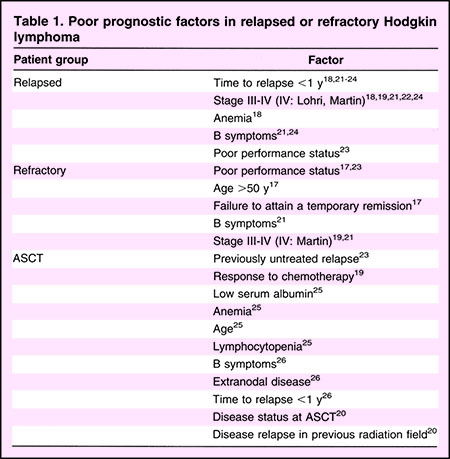
زمان عود بیماری نیز در پیشآگهی بیمار اهمیت زیادی دارد. با درنظرگرفتن این عوامل ما معتقدیم عود کمتراز۳ماه، دلالت بر مقاومبودن بیماری و ۳تا۱۲ماه نشانهی عود سریع میباشد که هردو گویای عاقبت بد هستند.
درمان:
بهرغم وجود انبوهی از انتشارات در بررسیهای فاز۲ برای درمان نجاتبخش(Salvage) جهت معالجهی عود و یا مقاومبودن بیماری هوچکین، مقایسهی مستقیمی روی رژیمهای مختلف درمانی صورتنگرفته و نظریهی اجماعی طلایی نیز دراینمورد ارائهنشده است. تجربهی اتفاقی کنترلشدهی منتشره در این خصوص و پیوند بنیاختههای اتولوگ (ASCT) توصیهی رژیم Mini-BEAM شـامل؛BCMU Etoposide,ara-C, Melphalan و یا پروتوکل Dexa BEAM مرکب از Dexamethosone. BCMU, Eloposide, Aea-Melphalan را رژیم استاندارد مینماید.
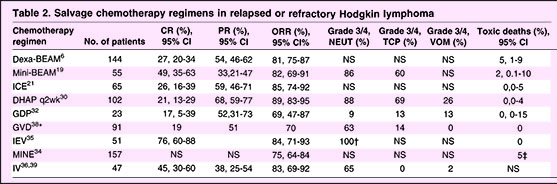
اگر هدفنهایی شیمیدرمانی نجاتبخش، رسیدن به پیوند اتولوگ (ASCT) باشد باید اخذ بهترین پاسخدرمانی با کمترین عارضهی خونی و غیرخونی قابلقبول باشد و صدمهای به جمعآوری بنیاختهها از خـونمحیـطی بــرایASCT نــزند. بــهاین دلیـل محققان به تجربهی اتفاقی کنتـرلشده (Randomized Controlled Triaial= RCT) درمورد استفاده از پروتکل Mini BEAM اعتقاد ندارند. ما نیز دریافتهایم که این پروتکل موجب سمیت هماتولوژیک مهمی بوده و نیازمند به بستریشدن متعدد بیماران در بیمارستان برای تب نوتروپنیک و وابستگی آنها به فرآوردههایخونی دارد و Mobilization بنیاخته را بهخطر میاندازد. رژیمهای متعدد وسیعی برای درمانSalvage انتشاریافته که خلاصهی آن در جدول۲ بهنظر میرسد. نتیجهی پاسخدرمانی با این پروتکلها بین۶۰تا۸۷ درصد است.
گرچه دراین بررسیها و تجارب، بیماران متفاوتی وجود داشته ولی هیچیک بر دیگری ارجحیت ندارد.بهطور معمول ۲دورهی پروتکل GDP شاملGemcitabine, Dexamethasone, Cisplatin را بهکارمیبریم و زمانیکه پاسخ درمانی را گرفتیم، به جمعآوری Stem Cell اقدام مینماییم.
بیمارانیکه از ابتدا به درمان مقــاوم باشند عاقبت بدتری نسبــتبه سایـــرین دارنــد (P>0.0001) (83% VS 51%).
متأسفانه فقدان پاسخدرمانی در شیمیدرمانی نجاتبخش (Salvage) کم نیست و پزشک درمانکننده را برسر دوراهی و تنگنا میگذارد. در تجربهی گروه آلمانی (GHSG) فقط بیمارانیکه پاسخ درمانی داده بودند و به ASCT دستیافتند، ملاک عمل نمیباشند. ما قبلاً در ۳۷بیمار مسن گرفتار RR.HL (بیماران دچار عود و یا مقاوم) گزارشکردیم که پروتکل dexamethasone high dose ava-c cisplatin بهکاررفت؛ از ۱۰تَن، ۶ بیمار که به پاسخ Sub Optimal دستیافته و وارد بهبودی نسبی (PR) شدند را برای پیوند ASCT فرستادیم. ما اخیراً تجربیات خود را درمورد بیمارانیکه به خاموشی کامل و یا بهبودی نسبی با پروتکلGDP نرسیده بودند ولی وضعیت خوب و ثابت دارند، منتشر نمودیم. Policy ما این است که وقتی مطمئن شدیم که آزمایشهای Imaging منفی است (توسط Gallium Scan) حجم توده را از ۵سانتیمتر کمترکنیم. پیوندASCT در ۹۹بیماری که خاموشی کامل (CR) و یا بهبودی نسبی(PR) داشتند را با ۱۳تَن که بیماری ثابت داشتند مقایسه کردیم؛ پاسخ درمانی بهترتیب ۶۱ و ۶۹درصد بود. یعنی تا ۵سال، عدم پیشرفت بیماری (PFS) فرقی نداشت.
در بیمارانیکه بیماری در وضعیت ثابت قراردارد و باقیماندهی آنومالی بیماری بعداز دریافت پروتکلGDP بیشاز ۵سانتیمتر است، ما پروتکل Mini-BEAM را بهکار میبریم. از این ۱۹بیماری که بهاندازهی کافی به پروتکلGDP جواب نداده بودند ۳۲درصد به این رژیم پاسخدرمانی را نشاندادند؛ گرچه با خصوصیات Criteria، ۴۷درصد از آنها پیوندASCT شدند، ۵سال عمر عاریاز پیشرفت بیماری (PFS) مأیوسکننده و ۲۲درصد بود. در سری بیماران ما ۱۰تَن از ۱۳۱بیمار (۸درصد) پاسخ درمانی کافی به شیمیدرمانی نداده و روی درمان Non Curative قرارگرفتند. نکتهی مهم مربوط به شیمیدرمانی نجاتدهنده (Salvage) در توانبخشی درمان دستدوم (Spcond line Therapy)، صدمه به موبیلیزاسیون بنیاختههای خونمحیطی است.
نتیجه:
بهرغم بررسیتصادفی کنترلشده (RCT) پایه و اساس درمان بیماری هوچکین مقاوم و یا عود شده، اختلاف نظر و بحث و مجادلهی زیادی دراینزمینه وجود دارد. با نگاه به آینده، یکیاز کلیدهای چالش در درمان عود و یا مقاومبودن بیماری به درمان (Chemorefractory) میباشد. گرچه پیوند Autorgafting ممکناست با موفقیت تعدادی از این بیماران را درمان قطعی نماید ولی در بررسیهای آیندهنگر بهخوبی معرفی نگردیده و بیولوژی زیربنایی بیماری روشن نشدهاست. مسلماً این یک زمینهای است که باید درآن تحقیقات اساسی صورتگیرد تا بهبودی در آیندهی بیماران را تضمین نماید. چالش دیگر برای پزشک معالجهکننده این است که خارج از بررسیهای RCT، کدام روش درمانی را برای این بیماران برگزیند و چگونه از Imaging و رادیوتراپی قبلاز پیوند بهره ببرد. گرچه تقریباً ۵۰درصد از بیماران بهبودی طولانی پیدامیکنند ولی امید است که استراتژی بهرهبری از Immunotherapy و یا داروهای نوین، قبلاز پیوندASCT در تجربیات کنترلشده برنامهریزی شود که همکاری بینالمللی دراین مورد لازم است.
Ref: John kuruvilla et al Blood How I Treat Relapsed and Refractory 2014 Hodgkin lymphoma













